Не патентуется? Спасибо, не надо.
По мнению одного из авторов британского журнала НьюСайнтист (New Scientist) давно известный лекарственный препарат Дихлорацетат (DCA) – это анти-раковое лекарство с огромным потенциалом, но без прибыли для фармакологических компаний. Здесь приводится реферат этой статьи.
Некоторые из противо-раковых лекарств появляются после лучшего понимания того, как развивается болезнь. Другие работают такими механизмами, которые мы не понимаем, и они дают нам свежий взгляд на проблему. Редко можно найти такое лекарство, которое годами ждет своего разрешения к применению и в то же время предполагает эффективное лечение всех форм болезни.
 Это лекарство – простая небольшая молекула, называемая дихлорацетат (ДХА = DCA). Исследования в Канаде, проведенные Эванделосом Мичелакисом в Университете Альберта в начале 2007 г., показали, что оно обладает замечательными противораковыми свойствами. И это еще не все! Механизм действия этого лекарства также вызывает восхищение.
Это лекарство – простая небольшая молекула, называемая дихлорацетат (ДХА = DCA). Исследования в Канаде, проведенные Эванделосом Мичелакисом в Университете Альберта в начале 2007 г., показали, что оно обладает замечательными противораковыми свойствами. И это еще не все! Механизм действия этого лекарства также вызывает восхищение.
В 1930 м году биохимик Отто Варбург предположил, что клетки становятся раковыми путем изменения способа получения энергии. В норме для обеспечения энергией клетки полагаются на специальные органеллы, называемые митохондриями. Раковые клетки переключаются на процесс, называемый гликолизом, который происходит внутри самой клетки. Это неэффектфивный процесс, используемый также бактериями, а также бегунами – марафонцами, когда кислорода в организме не хватает.
Удивительно, что Варбург нашел, что раковые клетки продолжают использовать гликолиз даже тогда, когда кислорода в достаточном количестве. Исследователь утверждал, что этот факт, сейчас называемый эффект Варбурга, является определяющей особенностью раковых клеток. Однако идея не прижилась возможно потому, что другой знаменитый биохимик Ханс Кребс считал, что эффект Варбурга был только симптомом рака, а не его исходной причиной. Это скептическое отношение было усилено тем, что раковые клетки переключаются на гликолиз только потому, что их митохондрии не работают.
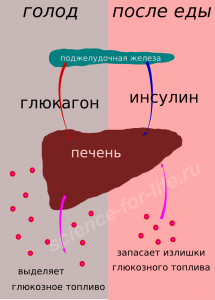
Со времен Варбурга многое в метаболизме клетки стало известно гораздо лучше благодаря тому, что наука не стоит на месте. Организм человека живет и функционирует засчет энергии, получаемой от потребления продуктов питания. Питательные вещества расщепляются на короткие молекулы, которые при соединении с кислородом выделяют энергию. Элементарная порция энергии в организме запасается в виде молекулы АТФ – энергетической разменной монеты, которая затем отдает энергию в нужном месте для процессов жизнедеятельности клетки. В нормальных клетках сжигание питательных молекул и формирование АТФ происходит в сложно устроенных органеллах – митохондриях. Это высокоэкономичный процесс, позволяющий клеткам эффективно использовать питательные вещества. Однако в раковых клетках митохондрии по какой-то причине повреждаются и не могут работать как энергеические станции клетки. Поэтому такая клетка переключаются на гликолиз – реакцию, при которой в просвете клетки расщепляется молекула глюкозы с образованием одной молекулы АТФ. Это неэффектфивный и расточительный процесс. При гликолизе образуется молочная кислота, которая разрушает коллагеновый матрикс, который соединяет клетки между собой. Такие ненормальные клетки покидают свое место и могут перемещаться в организме, образуя раковые опухоли в других частях тела – метастазы.
У митохондрий, как недавно обнаружили ученые, есть еще одна важная роль. Они запускают процесс апоптоза – естественной гибели клетки. Если митохондрии повреждены, то клетка становится бессмертной, то – есть раковой.
Вернемся к дихлорацетату, который использовался многие годы для лечения больных с митохондриальными болезнями, редкими расстройствами обмена веществ в организме. Это лекарство усиливает способность митохондрий вырабатывать энергию. Когда оно поступает в раковые клетки – происходит то же самое: по-видимому, митохондрии в раковых клетках не повреждены безвозвратно. И даже более того, работающая митохондрия помогает убить эти измененные раковые клетки. Это происходит из-за того, что восстановление работающих митохондрий отключает «бессмертие» раковых клеток.
Когда Мичелакис испытывал это лекарство на культуре раковых клеток, содержащихся в лаборатории, они погибали. Этот эффект был обнаружен по отношению к клеткам раковой опухоли легких, рака груди, рака головного мозга. Дихлорацетат не повреждал нормальные клетки. Когда это лекарство добавляли в воду, которую пили крысы с привитыми человеческими раковыми опухолями – опухоли значительно уменьшались. Получается, что Варбург был прав – гликолиз представляет собой что-то бльшее, чем просто симптом раковых клеток.
Интереснее всего то, что дихлорацетат выглядит как потенциальное противораковое средство. Оно дешевое, не повреждает нормальные клетки, мы хорошо знаем его побочные эффекты, и оно должно быть эффективно по отношению ко всем видам рака. Но есть одна проблема: это старое лекарство и оно не может быть запатентовано. Никакая фармацевтическая компания не захочет финансировать дорогостоящие клинические испытания без получения эксклюзивных прав производить и продавать лекарство.
Эта проблема не нова. Многие лекарства лежат на полках потому что компании не могут получить от них большую прибыль. Это случилось с лекарствами от болезней, которыми болеют бедные люди в развивающихся странах, таких как туберкулез, хотя сейчас и увеличивается сотрудничество между правительствами, благотворительными организациями и коммерческими компаниями для работы в этом направлении. В отличие от них рак – это болезнь богатых, и испытания дихлорацетата потребуют совершенно исключительных усилий.
Можно побиться об заклад о том, что фармацевтические компании приложат все усилия к тому, чтобы найти патентуемое соединение с таким же механизмом действия, как у дихлорацетата. Каждое из них, попавшее на рынок, будет очень дорогим. Но получится скандал, если дешевое альтернативное средство с такими замечательными свойствами не получит своего шанса просто потому, что оно не принесет достаточно большую прибыль.