Главные молекулы
1. Хеликаза
 Наследственная информация хранится в виде длинной молекулы ДНК, которая выглядит как двойная цепочка, закрученная в спираль.
Наследственная информация хранится в виде длинной молекулы ДНК, которая выглядит как двойная цепочка, закрученная в спираль.
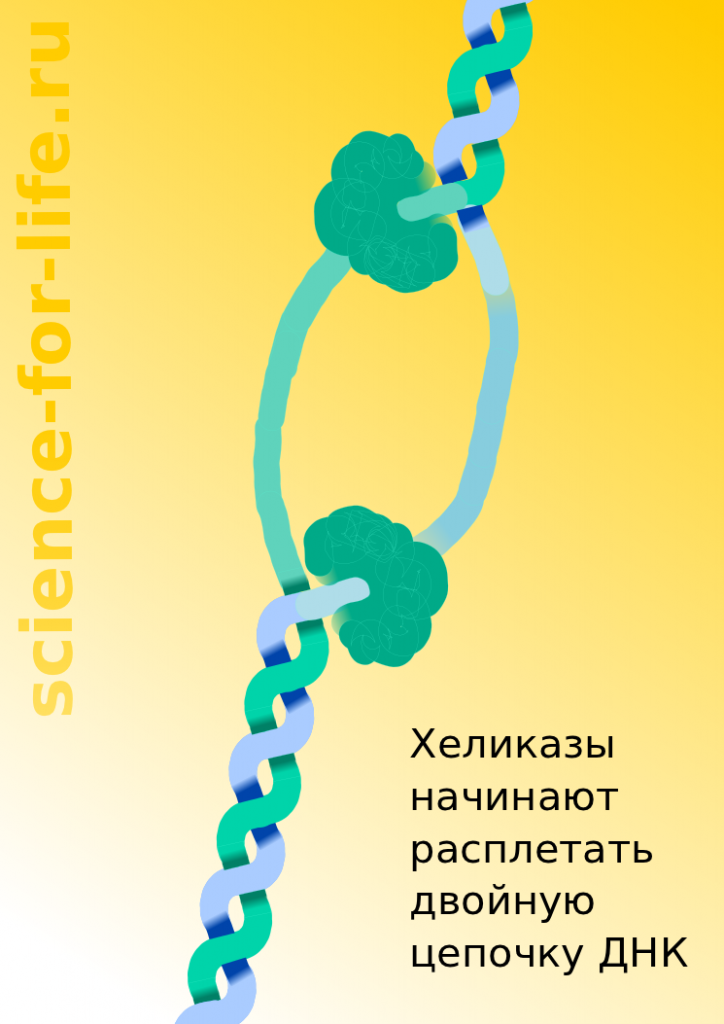
Для считывания информации или для удвоения наследственной информации при делении клетки необходимо разделить двойную молекулу ДНК на две отдельные цепочки. Клеточный фермент Хеликаза выполняет эту работу (См. Рис. Helicase).
В человеческих клетках встречается 24 разновидности Хеликаз. Они различаются способностью расплетать разные по составу двойные цепи нуклеиновых кислот, в том числе ДНК, и работать в разных направлениях. Отдельные Хеликазы изучены и их молекулярная структура расшифрована. Хеликазы состоят из трех или двух пар субъединиц, которые соединены так, что в центре между ними имеется отверстие.
Используя энергию АТФ, Хеликаза работает как «молекулярная машина», двигаясь вдоль цепочки ДНК и разделяя ее на две составные цепочки. При этом молекула Хеликазы совершает пульсирующие движения и одна из цепочек ДНК затягивается в отверстие в центре молекулы Хеликазы.
Лекарства, блокирующие активность Хеликазы, или, другими словами, ингибиторы Хеликазы, используются для лечения вирусного гепатита C и также планируются для полного искоренения этой болезни.
2. Рецептор фактора эпидермального роста EGFR
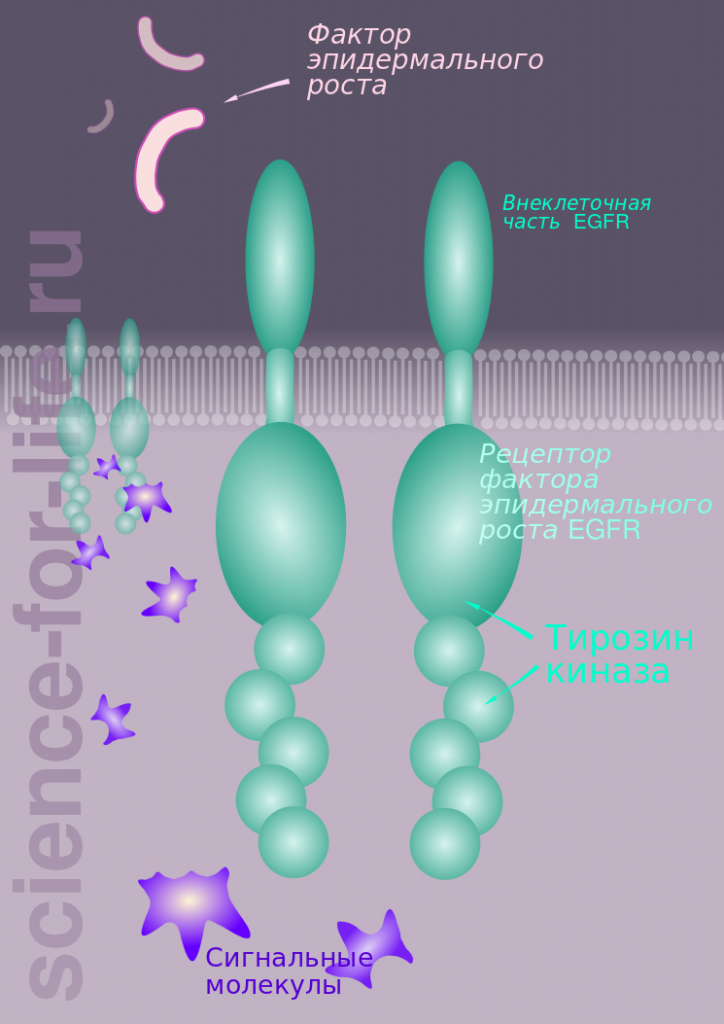 Эта молекула присутствует в нормальных клетках, но когда она в результате мутации появляется в большом количестве, то клетка становиться раковой и начинает безудержно делиться. Дело в том, что именно эта молекула получает из крови сигнал на деление и рост и передает этот ложный сигнал клетке, делая ее раковой. Поэтому ученые пытаются найти слабое звено в структуре этой важной молекулы, чтобы попытаться если не разрушить ее, то по крайней мере нарушить ее вредную работу. Например тирозин-киназа – часть этой молекулы (tyrosine kinase TK) и такие лекарства как Гефитиниб (gefitinib = Iressa) или Эрлотиниб (erlotinib = Tarceva) блокируют эту тирозин-киназу и делают страшную молекулу безвредной.
Эта молекула присутствует в нормальных клетках, но когда она в результате мутации появляется в большом количестве, то клетка становиться раковой и начинает безудержно делиться. Дело в том, что именно эта молекула получает из крови сигнал на деление и рост и передает этот ложный сигнал клетке, делая ее раковой. Поэтому ученые пытаются найти слабое звено в структуре этой важной молекулы, чтобы попытаться если не разрушить ее, то по крайней мере нарушить ее вредную работу. Например тирозин-киназа – часть этой молекулы (tyrosine kinase TK) и такие лекарства как Гефитиниб (gefitinib = Iressa) или Эрлотиниб (erlotinib = Tarceva) блокируют эту тирозин-киназу и делают страшную молекулу безвредной.
Рецептор фактора эпидермального роста EGFR относится к семейству рецепторов тирозин-киназ, в которое также входят HER2/erbB2 и HER3/erbB3. Все они являются привлекательными мишенями для стратегий лечения раковых заболеваний. EGFR – это сложная белковая молекула, которая закодирована в одном из генов. Было 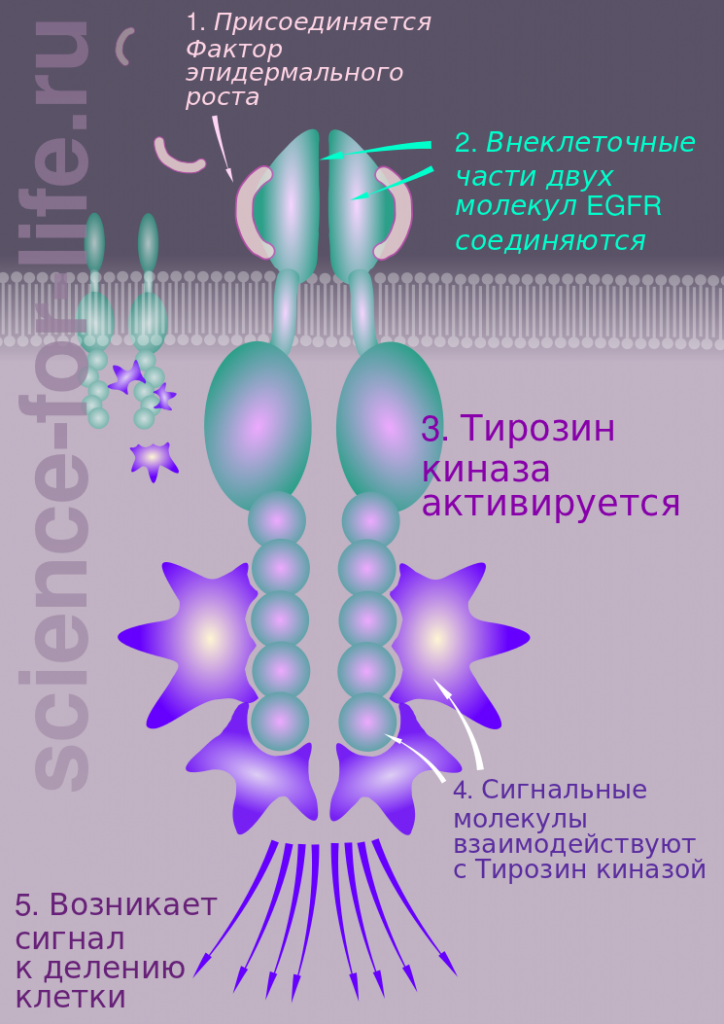 обнаружено, что больные немелкоклеточным раком легкого имеют мутацию в этом гене. Из-за этого в клетке начинается повышенный синтез белков на этом гене – суперэкспрессия. Такие больные, также как и другие, имеющие повышенное число EGFR в раковых клетках, хорошо лечатся целевыми лекарствами Гефитиниб и Эрлотиниб. Обнаружено также, что при лечении этими лекарствами у пациентов повышается число рецепторов EGFR, что по-видимому, обусловлено компенсаторным ответом других клеток на эти препараты, тем не менее раковые клетки успешно подавляются. Важно также, что лекарства Гефитиниб и Эрлотиниб также хорошо работают и у некоторых больных, у которых нет повышенного содержания вышеупомянутых рецепторов EGFR. Очевидно, что механизм действия этих лекарств более сложный, хотя главная мишень для них – это рецептор фактора эпидермального роста.
обнаружено, что больные немелкоклеточным раком легкого имеют мутацию в этом гене. Из-за этого в клетке начинается повышенный синтез белков на этом гене – суперэкспрессия. Такие больные, также как и другие, имеющие повышенное число EGFR в раковых клетках, хорошо лечатся целевыми лекарствами Гефитиниб и Эрлотиниб. Обнаружено также, что при лечении этими лекарствами у пациентов повышается число рецепторов EGFR, что по-видимому, обусловлено компенсаторным ответом других клеток на эти препараты, тем не менее раковые клетки успешно подавляются. Важно также, что лекарства Гефитиниб и Эрлотиниб также хорошо работают и у некоторых больных, у которых нет повышенного содержания вышеупомянутых рецепторов EGFR. Очевидно, что механизм действия этих лекарств более сложный, хотя главная мишень для них – это рецептор фактора эпидермального роста.
3. Вирус иммунодефицита человека ВИЧ
4. Эйкозапентаэноевая кислота
Эйкозапентаэноевая кислота – это одна из главных полиненасыщенных омега-3 жирных кислот. Жирные кислоты имеют простое строение. Они представляют собой цепочку из атомов углерода – главного строительного элемента живых организмов – и присоединенных к ним атомов водорода. С одного конца цепочки к углероду 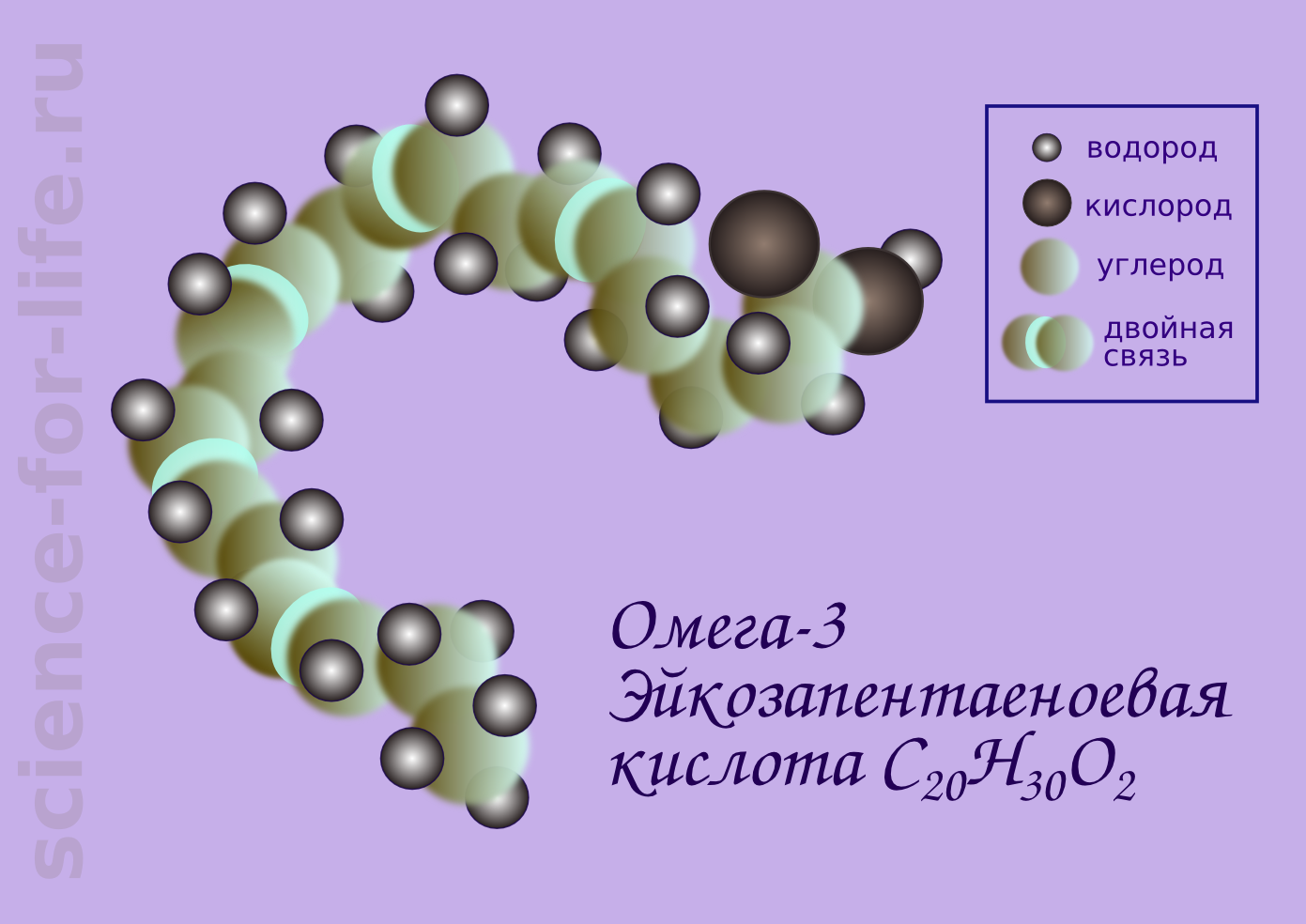 присоединены два атома кислорода в виде кислотной химической группы (см. схематическое изображение на рисунке). Три жирные кислоты, соединенные вместе с молекулой глицерина представляют собой молекулу жира. Две жирные кислоты, объединенные в молекулу фосфолипида, – это основной структурный элемент клеточных мембран. В клеточных мембранах обязательно должны быть ненасыщенные жирные кислоты. Они имеют изогнутую цепочку, потому клеточная мембрана, состоящая из таких жирных кислот становится более рыхлой и более устойчивой к химическим и физическим воздействиям.
присоединены два атома кислорода в виде кислотной химической группы (см. схематическое изображение на рисунке). Три жирные кислоты, соединенные вместе с молекулой глицерина представляют собой молекулу жира. Две жирные кислоты, объединенные в молекулу фосфолипида, – это основной структурный элемент клеточных мембран. В клеточных мембранах обязательно должны быть ненасыщенные жирные кислоты. Они имеют изогнутую цепочку, потому клеточная мембрана, состоящая из таких жирных кислот становится более рыхлой и более устойчивой к химическим и физическим воздействиям.
Больше всего ненасыщенных жирных кислот в тканях головного мозга. Человеческий организм плохо синтезирует ненасыщенные омега-3 жирные кислоты, и поэтому они должны поступать с пищей. Такие жирные кислоты содержатся в жире холодноводных океанических рыб – в жирном мясе семги, форели, горбуши и других видов красной рыбы, в сельди, мойве и др., а также в красной икре. Омега-3 жирные кислоты устойчивы к нагреванию, но постепенно разрушаются, окисляясь кислородом воздуха. Из полезного действия на организм человека пока научно доказанными являются два: 1) подавление воспаления в атеросклеротических бляшках в стенках кровеносных сосудов, что достоверно снижает смертность от инсультов и инфарктов; 2) повышение интеллекта и памяти, то есть улучшение работы головного мозга. Очевидно также, что омега-3 жирные кислоты представляют ценнейший компонент ежедневного питания человека.
5. Жирные кислоты в транс- и цис- конфигурации
В отличие от cis, trans конфигурация жирной кислоты означает, что следующие два атома углерода присоединены в противоположном направлении от двойной связи. В результате, они не образуют изгиб цепи и их форма похожа на насыщенные жирные кислоты. У большинства встречающихся в природе ненасыщенных жирных кислот каждая двойная связь имеет три атома углерода после нее, и все они представляют собой cis связи. Большинство жирных кислот в транс-конфигурации не найдены в природе и искусственно созданы человеком путем гидрогенизации.
6. Конъюгированные жирные кислоты
Конъюгированные жирные кислоты – это полиненасыщенные жирные кислоты, которые имеют две и более двойные связи, разделены только одной одиночной (одинарной) связью между атомами улгерода. Наиболее известны конъюгированные линолевые кислоты (английское сокращение CLA). Из известно более двух десятков изомеров. CLA обнаружены в основном в мясе и молочных продуктах, которые получены о жвачных животных (крупный рогатый скот, козы, овцы и др.). В мясе и молоке от животных, питающихся только травой на пастбище, в 3-5 раз больше CLA, чем у таких же животных, рацион которых состоит наполовину из силоса, наполовину из зерна. CLA в опытах на культурах раковых клеток проявили противоопухолевую активность, чем привлекли внимание общественности, фармацевтической и пищевой промышленности. Было также найдено, что цис-9, транс-11 форма CLA снижает риск сердечно-сосудистых болезней и лечит воспалительные процессы. В 2008 году Управление по продуктам питания и медикаментам США (FDA) выдало официальное подтверждение о безопасности CLA (GRAS статус) при добавлении ее в жидкое молоко, йогурт, фруктовые соки, соевое молоко и жидкие смеси-заменители и твердые съедобные составные продукты. Теперь производители продуктов питания могут добавлять CLA в продукты этих категорий. Однако существуют опасения, что употребление CLA людьми в состоянии значительного ожирения могут усиливать невосприимчивость к инсулину, чем увеличивать риск развития диабета.
Тем не менее CLA, по-видимому, не станет суперлекарством от рака. В январе 2010 г были опубликованы многолетние исследования Шведских ученых в которые были вовлечены 61 433 женщины. Снижение риска развития рака груди при употреблении диеты, богатой CLA не подтвердилось. Результаты даже указывают на слабую связь употребления CLA с увеличением риска развития рака груди. Один из изомеров – транс10, цис12 – рекомендуется избегать поскольку он может повреждать сердце и ускорять развитие опухолей молочных желез в экспериментах на лабораторных грызунах.
7. Цитотоксичные Т-лимфоциты (CTL)
Цитотоксичные Т-клетки (Cytotoxic T Lymphocytes: CTL) – это лимфоциты, которые убивают другие клетки, которые для них являются целевыми, т.е. на которые они нацелены, имея на своей поверхности антитела к антигенам, которые присутствуют на поверхности целевых клеток. Целями CTL являются инфицированные вирусом клетки, например инфицированные ВИЧ вирусом Т-лимфоциты, на которых присутвует белок CD4; целью может быть какже клетка, инфицированная бактериями или внутриклеточными паразитами; в-третьих, целью CTL может быть клетка пересаженного органа, например почки или сердца; в-четвертых, целью клеток-убийц CTL могут стать раковые клетки, хотя это обычно исключение, клетки CTL требуется изменить путем клеточной инженерии, чтобы они были нацелены на раковые клетки. С другой стороны, извращенная деятельность клеток CTL приводит к болезни сахарный диабет I типа, когда целью этих клеток-убийц становятся клетки, выделяющие инсулин островков Лангерганса в поджелудочной железе. Такие болезни называются аутоиммунными.
На поверхности клеток CTL находится рецептор, то-есть белок, который является антителом, специфическим к какому-то другому белку, который называется антиген. Рецептор отвечает за прикрепление клетки CTL к такой клетке, на поверхности которой находится целевой белок-антиген. Таким образом с помощью рецептора происходит навигация клетки-убийцы, иными словами с помощью рецептора CTL находит свою цель и прикрепляется к ней.
Как происходит разрушение целевой клетки, когда к ней присоединяется клетка CTL? Есть два пути: во-первых, прикрепившись к поверхности целевой клетки, CTL выделяет вещество, растворяющее наружную мембрану целевой клетки, и затем в образовавшиеся отверстия впрыскивается или яд – гранзим А, вызывающий остановку дыхания клетки, или вещество гранзим В, запускающее естественную гибель клетки – апоптоз. Второй путь уничтожения клетки – это выработка и введение в целевую клетку особого трансмембанного протеина, носящего название Fas ligand (FasL), который запускает апоптоз клетки.
